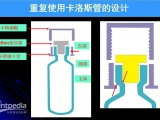
样品预处理
用5M盐酸胍以1:1的比例稀释200µL脑脊液(人脑脊液、猴脑脊液或加标人工脑脊液+5%大鼠血浆),并在室温下振摇45分钟。然后,用200µL 的4%H3PO4水溶液进一步稀释样品。
注意:对于加标样品而言,在加标后、用盐酸胍稀释前,可在室温下让样品平衡30分钟。
固相萃取(SPE)
基于µElution 96孔型的Oasis® MCX
预处理:200µL甲醇
平衡:200µL 4% H3PO4水溶液
上样:600µL预处理后的样品
清洗1:200µL 4% H3PO4水溶液
清洗2:10% ACN水溶液
洗脱:2×25µL 75:15:10 ACN:水:NH4OH浓溶液
稀释:25µL水
进样量:20µL
肽名称 | 前体离子 | 产物离子 | 产物离子ID | 锥孔电压(V) | 碰撞能量(eV) |
β淀粉样1-38肽 | 1033.5 | 1000.3 | b 36 | 33 | 23 |
β淀粉样1-38肽的N15内标 | 1046 | 1012.5 | 30 | 22 | |
β淀粉样1-40肽 | 1083 | 1053.6 | b 39 | 33 | 25 |
β淀粉样1-40肽的N15内标 | 1096 | 1066.5 | 35 | 22 | |
β淀粉样1-42肽 | 1129 | 1078.5 | b 40 | 28 | 30 |
β淀粉样1-42肽的N15内标 | 1142.5 | 1091.5 | 35 | 28 |
表1:β淀粉样肽及其N15标记型内标的MRM跃迁态和质谱条件

图2:β淀粉样1-42肽的典型ESI+MS/MS光谱
结果和讨论
开发这些方法所遇到的最大挑战就是克服溶解性、吸附性和聚集性问题并获得能满足该应用要求的足够选择性和灵敏度。适当的流动相和进样溶剂构成以及明智选择SPE洗脱溶剂仅仅是应对这些问题的几个关键因素。
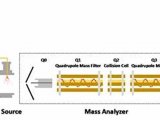
质谱分析
质谱分析在正离子模式下进行,因为4+前体的CID产生了几种与固有的特异性b序列离子相对应的不同产物离子(典型光谱如图2所示)。负离子模式下的MS/MS出现了明显的水分流失。图3给出了关于两种方法特异性区别的一个示例。虽然对于溶剂标准品时使用负离子模式的总体灵敏度较高,但在基质存在时负离子模式的灵敏度优势减弱,而正离子模式下的特异度和信噪比的提高对于脑脊液样品中的准确定量具有决定性作用。
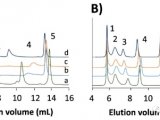
超高效液相色谱分析
图4显示了对这三种β淀粉样肽的分离情况。虽然流动相中NH4OH的精确百分比对负离子灵敏度具有关键作用,但ESI+模式下的信号经证实对流动相构成的细微变化更具稳健性,可使液相色谱/自动取样器至少在24小时以上的时间段中保持稳定。与此相反,50%或以上的ESI-信号在10-12小时后因流动相中NH4OH浓度的自然变化(挥发)而损失。这进一步强调了ESI+MS方法的稳健性。
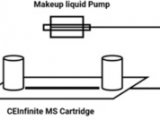
固相萃取(SPE)
SPE使用Oasis® MCX(一种混合模式的吸附剂)进行,以加强萃取过程的选择性。该吸附剂同时依赖于反相和离子交换保留机制,以从复杂脑脊液样品中的其它高丰度多肽中选择性分离β淀粉样肽组分。使用特定的96孔Oasis® µElution提供了明显的浓缩效果,无需溶剂挥干和复溶,从而尽可能减少了肽损失。此外,通过离子交换进行肽结合为整个方法提供了正交性。
在最初的方法开发过程中,萃取人工脑脊液时观察到了大量非特异性结合(NSB)。我们添加了5%大鼠血浆(有一个不同的β淀粉样肽序列),以消除NSB。
SPE是整个方法中较为重要的环节之一。对淀粉样组分选择性极高的分离再加上标准流速下UPLC的分辨率实现了对临床前研究样品的超快分析。