前言
细胞介导的免疫疗法的发展已经彻底改变了癌症研究和免疫系统研究。对新型嵌合抗原受体 (CAR) T 细胞进行基因工程改造,以靶向癌细胞,是具有前景的细胞治疗类型。尽管 CAR T 细胞疗法可能会使顽固性疾病患者得到持续缓解,但据近期试验报道,该疗法只对部分慢性淋巴细胞白血病 (CLL) 患者起作用[1]。目前,结果不理想的根本原因尚不明晰,然而获得性 T 细胞功能障碍可能是 CLL 病例出现这种状况的可能因素之一[2–5]。
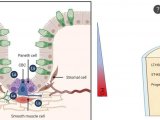
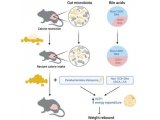
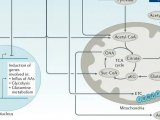
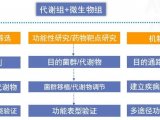
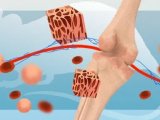
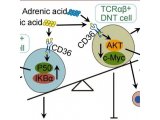
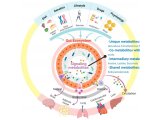
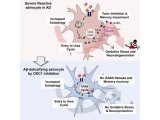
越来越多的人认识到 T 细胞功能和细胞代谢策略之间具有错综复杂的联系,这也提高了免疫细胞疗法结合代谢调节优化细胞产品,帮助患者获得更好疗效的价值[6–10]。如图 1 所示,静息 T 细胞主要凭借线粒体氧化磷酸化 (OXPHOS) 满足能量需求。T 细胞在活化后会立刻经历快速代谢重编程过程,对糖酵解和的依赖性提高,从而加速总体能量产生。这种转换使其能够迅速满足效应功能更多的能量需求[9]。代谢表型检测有助于针对代谢通路、代谢过程进行调节,以提高免疫细胞性能。
此前的研究已证实 CLL 患者的活化 CD8+ T 细胞表现出糖酵解障碍[11]。本应用简报总结了 Jaco van Bruggen 及其同事的一项研究,该研究旨在确定 CLL 细胞是否也会损害线粒体功能,因为 OXPHOS 在 T 细胞活化的早期事件中非常重要[5]。
研究结果
Jaco van Bruggen 等人使用安捷伦Seahorse XF 技术,证明了 CLL 患者的CD8+ T 细胞具有不稳定的代谢特征,线粒体功能减弱与这种代谢特征有关。与来自健康供体的 CD8+ T 细胞相比,CLL患者的静息 CD8+ T 细胞耗氧率 (OCR) 较高。他们还证明,OXPHOS 的这一提升与线粒体质量增大无关(图 1)[5]。
此外,CLL 患者的 CD8+ T 细胞与来自健康供体的细胞相比,备用呼吸能力 (SRC)更弱[5]。SRC 是一项有效可靠的线粒体功能衡量标准以及成熟有力的免疫细胞命运和适应性指标[7,12]。SRC 减弱表明 CLL 患者的 CD8+ T 细胞对 T 细胞活化等因素导致的生物能量需求变化的响应能力降低。
van Bruggen 及其同事还对转移 CAR T 细胞是否可以观察到与自体 CD8+ T 细胞类似的代谢适应性减弱提出了疑问。他们分析了 CAR T 细胞试验受试者中27 名复发性/顽固性 CLL 患者的注射产物中的 CAR+CD8+ T 细胞。有趣的是,随后呈现完全响应的病例与无响应者相比,注射的 CD8+ CAR T 细胞具有更大的线粒体质量。该发现与此前的一项研究一致 ― 氧化代谢特征为 T 细胞持久性提供了支持[13]。

图 1. 活化 T 细胞代谢策略。健康 T 细胞在活化后会立刻经历快速代谢重编程过程,对糖酵解依赖性提高,以满足更高的能量需求。研究表明,慢性淋巴细胞白血病 (CLL) 患者的 T 细胞中糖酵解和氧化磷酸化受损可能导致 T 细胞功能障碍。图片摘自 van Bruggen et al. 2019[5]

图 2. CLL 患者的 CD8+ T 细胞的线粒体代谢发生改变。使用安捷伦 Seahorse XF 分析仪分析 CLL 患者和年龄匹配健康供体的 PBCMs 以确定 OCR(表示OXPHOS;CLL,n = 7;HD,n = 6)。SRC 为最大 OCR 和基础 OCR 之比(CLL,n = 6;HD,n = 6)。图片摘自 van Bruggen et al. 2019[5]
作者据研究推测,线粒体健康受损可能是CLL 患者 T 细胞功能障碍的主要成因[5]。因此,免疫细胞的代谢健康与抗肿瘤有效性存在内在联系,是一项关键的决定因素。分析免疫细胞代谢对了解抗肿瘤免疫响应的生物学信息和疗法设计都至关重要。
结论
这项工作为表明代谢过程对免疫细胞命运、适应性和功能重要性的大量研究提供了佐证。安捷伦 Seahorse XF 技术是公认的研究免疫细胞代谢的前沿技术,可实时进行灵敏的代谢测量。能够为免疫细胞功能关键驱动因素的研究和细胞治疗产品的优化提供明确信息。安捷伦现提供Seahorse XF T 细胞代谢分析试剂盒,以更强大的试剂和更简单的测定工作流程,帮助您开发细胞疗法。使用该试剂盒,您可以进行与 T 细胞治疗产品的抗肿瘤特性相关的测量,全面了解 T 细胞能量代谢。
参考文献
1. Porter, D. L. et al. Chimeric Antigen Receptor T Cells Persist and Induce Sustained Remissions in Relapsed Refractory Chronic Lymphocytic Leukemia. Sci. Transl. Med. 2015,7(303), 303ra139
2. Riches, J. C.; Gribben, J. G.Understanding the Immunodeficiency in Chronic Lymphocytic Leukemia:Potential Clinical Implications.Hematol. Oncol. Clin. North Am. 2013,27(2), 207–35
3. te Raa, G. D. et al. Chronic Lymphocytic Leukemia Specific T Cell Subset Alterations Are CloneSize Dependent and not Present in Monoclonal B Lymphocytosis. Leuk.Lymphoma 2012, 53(11), 2321–5
4. Tonino, S. H. et al. Expansion of Effector T Cells Associated with Decreased PD-1 Expression in Patients with Indolent B Cell Lymphomas and Chronic Lymphocytic leukemia. Leuk.Lymphoma 2012, 53(9), 1785–94
5. van Bruggen, J. A. C. et al. Chronic Lymphocytic Leukemia Cells Impair Mitochondrial Fitness in CD8+ T Cells and Impede CAR T Cell Efficacy. Blood 2019, 134(1), 44–58
6. van der Windt, G. J. et al. CD8 Memory T Cells Have a Bioenergetic Advantage That Underlies Their Rapid Recall Ability. Proc. Natl. Acad.Sci. USA 2013,110(35), 14336–41
7. van der Windt, G. J. et al.Mitochondrial Respiratory Capacity Is a Critical Regulator of CD8+ T Cell Memory Development. Immunity 2012, 36(1), 68–78
8. Geltink, R. I. K.; Kyle, R. L.;
Pearce, E. L. Unraveling the Complex Interplay Between T Cell Metabolism and Function. Annu. Rev. Immunol.2018, 36, 461–488
9. Chang, C. H. et al. Posttranscriptional Control of T Cell Effector Function by Aerobic Glycolysis. Cell 2013, 153(6),1239–51
10. Buck, M. D.; O’Sullivan, D.;
Pearce, E. L. T Cell Metabolism Drives Immunity. J. Exp. Med. 2015, 212(9),1345–60
11. Siska, P. J. et al. Suppression of Glut1 and Glucose Metabolism by Decreased Akt/mTORC1 Signaling Drives T Cell Impairment in B Cell Leukemia. J. Immunol. 2016, 197(6),2532–40
12. The Central Role of Immune Cell Metabolism in Building NextGeneration Cell Therapies. Agilent Technologies, 2021
13. Distinct Signaling of Coreceptors Regulates Specific Metabolism Pathways and Impacts Memory Development in CAR T Cells.Immunity 2016, 44, 380–390
仅供科研使用,不用于临床诊断用途。
 长按识别二维码,关注安捷伦细胞分析
长按识别二维码,关注安捷伦细胞分析点击阅读原文了解更多信息